[!abstract] Daftar Isi
- Pengenalan Alat Kimia
- Metode Ilmiah
- Teori Atom
- Democritus
- John Dalton
- Joseph John Thomson
- Ernest Rutherford
- Niels Bohr
- Sistem Periodik Unsur
- Golongan
- Perioda
- Bilangan Kuantum
- Tata Nama Senyawa
- Persamaan Reaksi
1. Pengenalan Alat Kimia§
Bisa searching di Google 😊
Cari aja gambar-gambar alat kimia, muncul nanti
- Beaker atau gelas piala.
- Gelas ukur.
- Corong gelas.
- Pengaduk kaca.
- Karet pengisap.
- Pipet ukur.
- Labu ukur.
- Erlenmeyer.
- Tabung reaksi.
- Buret.
Kenapa alat kimia umumnya kaca?
Karena bening, lebih mudah untuk meneliti; tahan terhadap korosi; stabil pada suhu tinggi; mudah dibersihkan.
2. Metode Ilmiah§
Langkah-langkah sistematis untuk menyelesaikan masalah.
- Merumuskan masalah.
- Mengkasi teori.
- Membuat hipotesis.
- Merancang dan melakukan eksperimen.
- Mengolah dan menganalisis data.
- Menarik kesimpulan.
- Menulis laporan.
3. Teori Atom§
3.1. Democritus
Democritus percaya bahwa alam semesta terbuat dari ruang kosong dan bagian-bagian kecil yang ia sebut sebagai atom yang tidak dapat dibagi lagi menjadi bagian yang lebih kecil.
Atom berasal dari kata ‘atomos’ yang berarti tidak dapat dibagi.
3.2. John Dalton

- Materi terdiri dari atom yang tidak dapat dibagi lagi.
- Atom dari unsur kimia tertentu memiliki sifat yang sama.
- Unsur kimia berbeda akan memiliki jenis atom berbeda juga.
- Selama reaksi kimia, atom-atom hanya dapat bergabung dan dipecah menjadi atom-atom yang terpisah; tetapi atom tidak dapat dihancurkan dan tidak dapat diubah selama reaksi kimia tersebut.
- Suatu senyawa terbentuk dari unsur-unsur melalui penggabungan atom tidak sejenis dengan perbandingan yang sederhana.
3.3. Joseph John Thomson
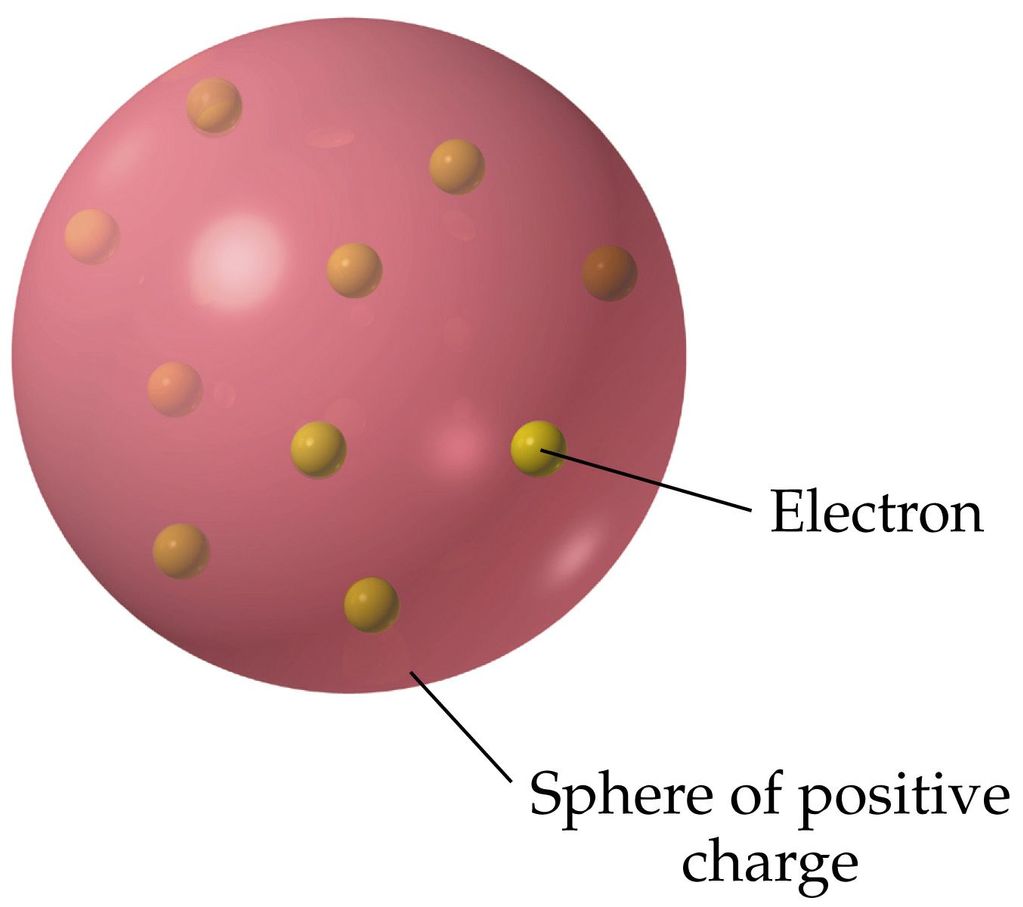
Dijuluki dengan model ‘roti kismis’ di mana elektron (bermuatan negatif) pada suatu bola pejal[^1] (bermuatan positif) dianggap seperti ‘kismis yang tersebar di atas roti.’
[^1]: pejal berarti padat tak berongga.
Model ini menggantikan teori Dalton yang menyatakan bahwa atom tidak dapat dibagi lagi.
Thomson menemukan elektron melalui sinar katode.


Jika penasaran apa itu sinar katode, baca Teori atom § Penemuan partikel subatomik.
3.4. Ernest Rutherford
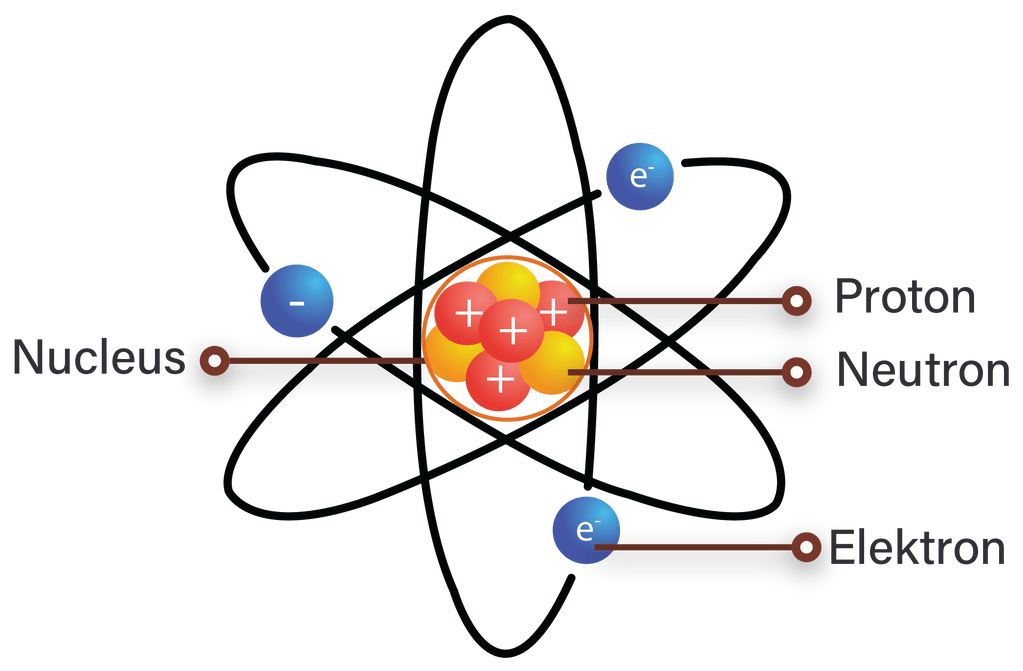
Model Rutherford menjelaskan bahwa atom
- memiliki inti bermuatan positif, padat, dan kecil di tengahnya; dan
- memiliki elektron bermuatan negatif yang mengorbit inti, seperti planet mengorbit matahari.
Diperkirakan jari-jari atom $\pu{10^{-8} cm}$ dan jari-jari inti atom $\pu{10^{-13} cm}$. Di antara inti dan elektron adalah ruang hampa.

Hasil ini didapat dari eksperimen hamburan sinar (partikel) alfa ke lempeng tipis, dengan tujuan pembuktian teori Thomson.
Partikel alfa adalah inti dari atom helium—atau $\ce{He^2+}$—yang memiliki dua proton dan dua neutron, membuat mereka bermuatan positif.
Rutherford berharap partikel alfa dapat melewati kertas logam tanpa pembelokan. Ternyata tidak, mereka menemukan partikel alfa mengalami pembelokan yang tajam.
Ia berkesimpulan bahwa muatan positif atom harus terkonsentrasi dengan volume yang sangat kecil karena dapat membelokkan partikel alfa (yang sama-sama positif, maka mereka saling tolak-menolak).
[!tip] Intinya … Teori atom Rutherford menyatakan
- Atom terdiri dari inti atom (+); dan
- elektron (−) yang mengorbit inti.
- Berdasar eksperimen sinar alfa ke lembaran emas tipis.
3.5. Niels Bohr
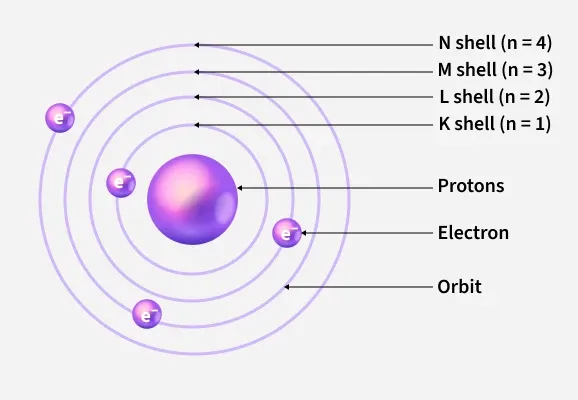
Elektron mengelilingi inti atom pada lintasan tertentu yang tetap, yang disebut sebagai orbit atau kulit.
Elektron tersebut dapat berpindah kulit dengan memancarkan/menyerap energi.
- Untuk ke kulit yang lebih dekat ke inti, elektron memancarkan energi.
- Untuk ke kulit yang lebih jauh dari inti, elektron menyerap energi.
Teorinya berdasarkan pada penelitian terhadap spektrum atom, terutama spektrum atom hidrogen.
Kulit-kulit diberi nama K, L, M, dan seterusnya. Setiap kulit ke-$n$ hanya dapat ditempati maksimal $2n^2$ elektron.
Kulit K, L, dan M akan diisi dulu dari awal. Penuhkan dulu K, baru L. Lalu penuhkan L, baru M.
Walaupun begitu, kulit N sudah akan terisi apabila M sudah mencapai 8 elektron.
Misalnya untuk magnesium $\ce{_12Mg} : 2 \quad 8 \quad 2$.
Sedangkan untuk kalium $\ce{_19K} : 2 \quad 8 \quad 8 \quad 1$.
*Dari kiri ke kanan: dari yang paling dekat dengan inti ke yang paling jauh.
4. Sistem Periodik Unsur (SPU)§
Untuk tabel periodik interaktif, bisa gunakan Ptable
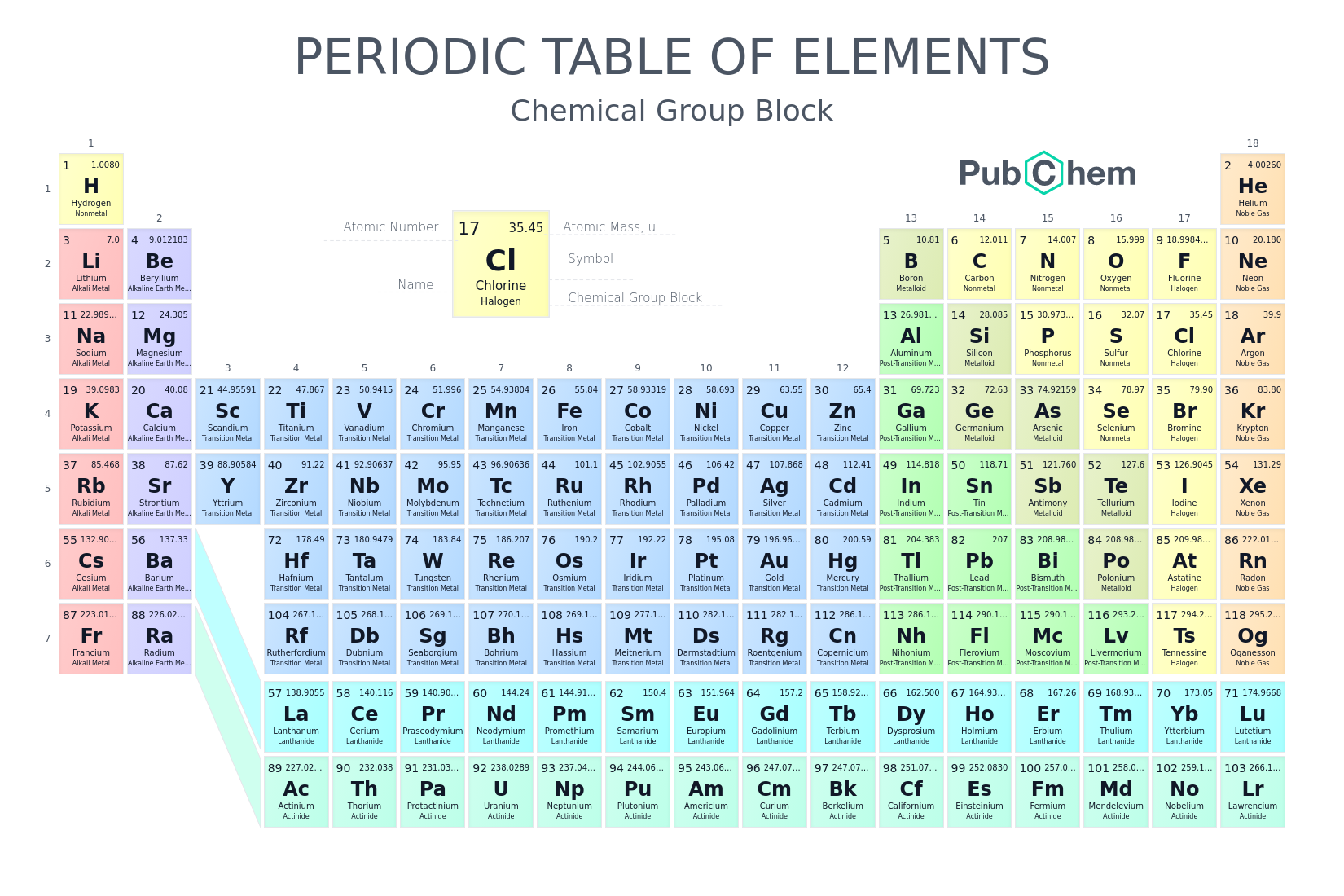
Tabel periodik adalah tabel untuk unsur-unsur kimia. “Periodik” karena satu baris (horizontal) disebut satu periode. Satu kolom (vertikal) disebut satu golongan.
Periode dan golongan ini ditentukan dari konfigurasi elektron atom tersebut.
Dari kiri ke kanan ada 18 golongan:
- IA dan IIA.
- IIIB sampai VIIIB.
- IB dan IIB.
- IIIA sampai VIIIA.
Golongan VIIIB mencakup 3 kolom.
Dari atas ke bawah ada 7 periode.
Konfigurasi elektron yang digunakan adalah subkulit. Subkulit ada 4: s, p, d, dan f.
Subkulit dapat memuat beberapa elektron.
- Subkulit $\ce{s}$ maksimal 2 elektron.
- Subkulit $\ce{p}$ maksimal 6 elektron.
- Subkulit $\ce{d}$ maksimal 10 elektron.
- Subkulit $\ce{f}$ maksimal 14 elektron.
Penulisannya:
- Didepan subkulit adalah nomor kulit.
- Sedangkan angka di atas kanan (pangkat) adalah banyak elektron pada subkulit tersebut.

Untuk menentukan konfigurasi elektron, urutannya mengikuti
- $\ce{1s}$
- $\ce{2s 2p}$
- $\ce{3s 3p 3d}$
- $\ce{4s 4p 4d 4f}$
- $\ce{5s 5p 5d 5f}$
- $\ce{6s 6p 6d}$
- $\ce{7s 7p}$
dengan pola diagonal. (Lihat gambar di samping).
Isi dari paling awal menurut pola tersebut.
Sebagai contoh klorida $\ce{_17Cl} : \ce{1s^2 2s^2 2p^6 3s^2 3p^5}$.
Untuk nomor atom yang masih kecil, ini masih aman, tapi kalau nomor atomnya 87 bagaimana?
Ada namanya penyingkatan, yaitu kita pakai unsur yang paling stabil (gas mulia, atau golongan VIIIA).
Untuk klorida $\ce{_17Cl}$ tadi, unsur yang paling dekat dengan $\ce{_17Cl}$ namun masih di bawahnya adalah neon $\ce{_10Ne}$.
Karena $\ce{_10Ne} : \ce{1s^2 2s^2 2p^6}$, substitusikan kepada konfigurasi tadi.
Maka $\ce{_17Cl} : \ce{[Ne] 3s^2 3p^5}$.
Untuk menentukan letak suatu unsur, dicarilah golongan dan periodenya, semacam “koordinat” pada tabel periodik.
4.1. Golongan
Golongan ada bagian angka dan hurufnya.
Untuk golongan(hu.) A:
- Berakhir pada subkulit $\ce{s}$ atau $\ce{p}$
- Jika berakhir pada subkulit $\ce{s}$, maka golongan(an.)nya adalah jumlah elektron di subkulit $\ce{s}$.
- Jika berakhir pada subkulit $\ce{p}$, maka golongan(an.)nya adalah jumlah elektron di subkulit $\ce{p}$ dan $\ce{s}$.
Untuk golongan(hu.) B:
- Berakhir pada subkulit $\ce{d}$.
- Pertama, jumlahkan elektron di subkulit $\ce{s}$ dan $\ce{d}$.
- Jika jumlahnya 3 sampai 7, maka golongan(an.) mengikuti.
- Jika jumlahnya 8 sampai 10, maka golongannya VIIIB.
- Jika jumlahnya 11 maka golongannya IB.
- Jika jumlahnya 12 maka golongannya IIB.
Untuk akhiran subkulit $\ce{f}$:
- Jika $\ce{4f}$ maka golongan lantanida.
- Jika $\ce{5f}$ maka golongan aktinida.
Sebagai contoh, klorida $\ce{_17Cl} : \ce{[Ne] 3s^2 3p^5}$.
- Berakhir pada subkulit $\ce{p}$ maka golongan A.
- Jumlahkan $\ce{p}$ dan $\ce{s}$ menjadi $7$.
- Maka $\ce{_17Cl}$ pada golongan VIIA.
4.2. Perioda
Perioda adalah bilangan kulit terbesar yang ada.
Contohnya $\ce{_17Cl} : \ce{[Ne] 3s^2 3p^5}$, bilangan kulit terbesarnya adalah $3$. Maka $\ce{_17Cl}$ berada di periode 3.
Contoh lain besi $\ce{_26Fe} : \ce{[Ar] 4s^2 3d^6}$. Bilangan kulit terbesarnya adalah $4$. Maka besi berada di periode 4.
5. Bilangan Kuantum§
Ada 4 bilangan kuantum.
Biasanya akan ditanya bilangan kuantum subkulit terakhir.
5.1. Utama $(n)$
Bilangan kuantum (bk.) utama adalah nomor kulit.
Sebagai contoh $\ce{}$$\ce{}$$\ce{3p^5}$. Bk. utamanya adalah $n = 3$.
5.2. Azimut $(\ell)$
Anggap subkulit dinomori dari $0$ hingga $3$. Di mana $\ce{s} \rightarrow 0$ hingga $\ce{f} \rightarrow 3$.
Maka bk. azimut adalah nomor urut tersebut.
Sebagai contoh $\ce{3p^5}$. Bk. azimutnya adalah $\ell = 1$.
5.3. Magnetik $(m)$
Banyak bilangan yang ada di antara $-\ell$ hingga $\ell$ (inklusif).
Sebagai contoh $\ce{3p^5}$. Karena $\ell = 1$, bilangan dari $-\ell$ hingga $\ell$ ada $-1, 0, 1$. Maka bk. magnetiknya adalah $m = -1, 0, 1$.
Bk. magnetik menyatakan banyak orbital, yaitu “kamar” untuk elektron. Di mana satu orbital dapat menampung 2 elektron.
Elektron diisi dari $-\ell$ dulu satu per satu.
Misalkan untuk $\ce{3p^5}$. Bk. magnetik elektron terakhirnya adalah $m = 0$. Karena pengisian mulai dari $-1$, $0$, $1$, balik lagi $-1$, $0$.
5.4. Spin $(s)$
Spin adalah arah elektron terakhirnya.
Spin bernilai $s = +\dfrac{1}{2}$ atau $s = -\dfrac{1}{2}$.
Karena pengisian elektron ada dua siklus, maka siklus pertama $s = +1/2$ dan siklus kedua $s = -1/2$.
Pada contoh $\ce{3p^5}$, elektron terakhir jatuh di siklus kedua, maka $s = -1/2$.
6. Tata Nama Senyawa§
Sebelum itu, banyak atom pada suatu senyawa dinyatakan dengan angka di kanan bawah atom. Contohnya, air $\ce{H2O}$, memiliki 2 atom hidrogen $\ce{H}$ dan 1 atom oksigen $\ce{O}$. Angka 1 tidak perlu ditulis.
Atom bisa ‘bersatu’ karena muatannya berbeda. Misalkan negatif dengan positif.
Atom bermuatan negatif (−) disebut sebagai anion dan atom bermuatan positif (+) disebut sebagai kation.
- (−) — Anion
- (+) — Kation
6.1. Nama Senyawa Ion
Nama kation disebut terlebih dahulu.
Sebagai contoh ion natrium $\ce{Na+}$ dan ion klorin $\ce{Cl-}$
$$ \ce{Na+ + Cl- -> NaCl} $$
akan disebut sebagai natrium klorida (atau garam dapur).
Untuk ion monoatomik (satu unsur), bisa lihat gambar berikut.

Penyebutan namanya akan sama dengan nama aslinya, kecuali unsur tersebut memiliki beberapa jenis ion, seperti besi $\ce{Fe}$ dan tembaga $\ce{Cu}$.
Besi memiliki dua ion, yaitu $\ce{Fe^2+}$ dan $\ce{Fe^3+}$. Untuk hal ini, tambahkan jumlah ionnya setelah namanya, contoh “besi(II)” dan “besi(III)”.
Maka $\ce{Fe^2+ + Cl- -> FeCl_2}$ disebut sebagai “besi(II) klorida”.
Untuk kata kedua, ditambahkan akhiran “-ida”:
- Klorin menjadi klorida.
- Oksigen menjadi oksida.
- Karbon menjadi karbida.
- dan seterusnya.
Untuk ion poliatomik, bisa lihat tabel berikut. (Hanya sebagian ion saja)
| Rumus | Nama Ion |
|---|---|
| $\ce{NH4+}$ | amonium |
| $\ce{H3O+}$ | hidronium |
| $\ce{NO2+}$ | nitronium |
| $\ce{CN-}$ | sianida |
| $\ce{OH-}$ | hidroksida |
| $\ce{SCN-}$ | tiosianat |
| $\ce{MnO4-}$ | permanganat |
| $\ce{CrO4^2-}$ | kromat |
| $\ce{Cr2O7^2-}$ | dikromat |
| $\ce{C2H3O2-}$ atau $\ce{CH3COO-}$ | asetat |
| $\ce{S2O3^2-}$ | tiosulfat |
| $\ce{SiO3^2-}$ | silikat |
| $\ce{C2O4^2-}$ | oksalat |
| $\ce{CO2^2-}$ | karbonit |
| $\ce{CO3^2-}$ | karbonat |
| $\ce{NO2-}$ | nitrit |
| $\ce{NO3-}$ | nitrat |
| $\ce{SO3^2-}$ | sulfit |
| $\ce{SO4^2-}$ | sulfat |
| $\ce{PO3^3-}$ | fosfit |
| $\ce{PO4^3-}$ | fosfat |
| $\ce{AsO3^3-}$ | arsenit |
| $\ce{AsO4^3-}$ | arsenat |
| $\ce{ClO-}$ | hipoklorit |
| $\ce{ClO2-}$ | klorit |
| $\ce{ClO3-}$ | klorat |
| $\ce{ClO4-}$ | perklorat |
Susah menghapalnya?
[!tip] Intinya …
- Untuk akhiran “-at” dan “-it”
- “-at” → jumlah $\ce{O}$ lebih banyak.
- “-it” → jumlah $\ce{O}$ lebih sedikit.
- Bentuk “hipo-…-it”
- Jumlah $\ce{O}$ hanya 1.
- Bentuk “per-…-at”
- Jumlah $\ce{O}$-nya banyak (≥ 3).
- Urutannya “hipo-…-it” — “-it” — “-at” — “per-…-at”
- Jika mengandung hidrogen $\ce{H}$
- Tambahkan “hidrogen”
Untuk menentukan rumus senyawanya. Silangkan dan turunkan ionnya.
Misalkan magnesium dan natrium $\ce{Mg^2+ + N^3-}$.
- Silangkan dan turunkan ion $2+$ kepada $\ce{N}$ → $\ce{N2_+}$.
- Silangkan dan turunkan ion $3-$ kepada $\ce{Mg}$ → $\ce{Mg3_-}$.
- Buang tandanya.
- Sehingga hasilnya $\ce{Mg3N2}$ (magnesium nitrida).
$$ \ce{Mg^2+ + N^3- -> Mg3N2} $$
Sama untuk unsur poliatomik.
Sebagai contoh, amonium $\ce{NH4+}$ dan kromat $\ce{CrO4^2-}$.
- Ion $+$ ke $\ce{CrO4}$ → $\ce{(CrO4)_+}$.
- Ion $2-$ ke $\ce{NH4}$ → $\ce{(NH4)2_-}$.
- Buang tanda.
- Menjadi $\ce{(NH4)2CrO4}$ (amonium kromat).
$$ \ce{NH4+ + CrO4^2- -> (NH4)2CrO4} $$
7. Persamaan Reaksi§
Untuk menyamakan reaktan (ruask kiri) dan produk (ruas kanan), kita perlu menambahkan koefisien unsur.
Caranya? Ya …, tinggal coba-coba saja 😊, sampai dapat hasil yang tepat (jumlah unsur di reaktan sama dengan jumlah unsur di produk).